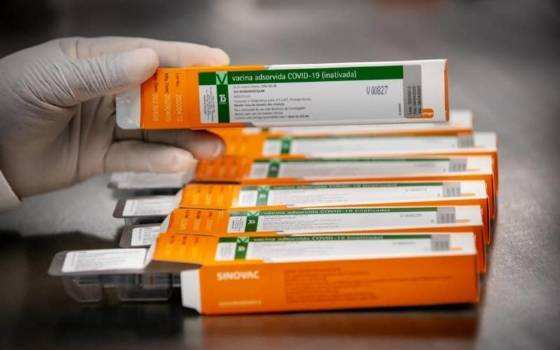
A Anvisa autorizou a retomada do estudo clínico relacionado à vacina CoronaVac, que tem como patrocinador o Instituto Butantan. A Agência informou que havia suspendido na última segunda-feira (09.11) a medida, de caráter exclusivamente técnico, porque levou em consideração os dados que eram do conhecimento da Anvisa até aquele momento - e os preceitos científicos e legais que devem nortear as ações, especialmente o princípio da precaução, que prevê a prudência, a cautela decisória quando o conhecimento científico não é capaz de afastar a possibilidade de dano.
Conforme a Anvisa, após avaliar os novos dados apresentados pelo patrocinador depois da suspensão do estudo, entendeu que tem subsídios suficientes para permitir a retomada da vacinação e segue acompanhando a investigação do desfecho do caso para que seja definida a possível relação de causalidade entre o EAG inesperado e a vacina.
“É importante esclarecer que uma suspensão não significa necessariamente que o produto sob investigação não tenha qualidade, segurança ou eficácia. A suspensão e a retomada de estudos clínicos são eventos comuns em pesquisa clínica e todos os estudos destinados a registro de medicamentos que estão autorizados no país são avaliados previamente pela Anvisa com o objetivo de preservar a segurança dos voluntários do estudo”, ressalta a Anvisa.
Por fim, a Anvisa reitera que trabalha para garantir o acesso a produtos e serviços seguros e eficazes, pautando-se na avaliação benefício-risco e no equilíbrio entre os princípios da legalidade, transparência, precaução e razoabilidade de suas ações.
Entre no grupo do VGNotícias no WhatsApp e receba notícias em tempo real (CLIQUE AQUI).